
 |
身近な物質を教材としたカルシウム化合物の授業
富山県立富山高等学校
横田 淳一
1.はじめに
「理科の学習において基礎的・基本的な知識・技能は,実生活における活用や論理的な思考力の基盤として重要な意味を持っている」しかし「国際的に見ると,我が国の子どもたちの理科に対する意欲は低い状況が見られる」また「理科の学習の基盤となる自然体験,生活体験が乏しくなっている状況が見られる。」(中央教育審議会 初等中等教育分科会 教育課程部会「教育課程部会におけるこれまでの審議のまとめ」(平成19年11月7日)より)
そこで,身近な物質を通して化学を学べば乏しくなった生活体験を補い,実生活においても化学的視点からものごとを見ることができるようになり,理科に対する意欲が高まると考えた。
本実践では,骨の主成分元素であり,脊椎動物に欠かすことのできないものであるカルシウムを取り上げた。はじめに,身近に多数あるカルシウム化合物を通して化学を楽しく学ぶことができる教材を開発した。次に,その教材を用いた授業を実践した。さらに,その授業で興味を持った生徒達が課題研究にも取り組んだ事例を報告する。
2.テーマ設定の理由
(1)カルシウムとその化合物を学ぶ意義
私たちは,自然界の中で生活している。この自然界は,金属・非金属合わせて約100種類の元素で構成された物質でできている。人間もその中の一員である。したがって物質について知ることは,私たち自身を知ることにもなる。
利用という点だけからなら,鉄を始めとしてアルミニウム・銅・金・銀・白金・ニッケル・コバルトなどの元素について学ぶことが重要である。しかし,もっと根本的に,私たちが生物として健康に生存していくという点から学ぶとしたら,ナトリウム・カリウム・マグネシウム・カルシウムとアルミニウム・鉄が最も重要な元素である。例えば,カルシウムは脊椎動物にとって,骨の主成分として欠かすことのできない元素である。
また,アルカリ金属元素とアルカリ土類金属元素は,化学的性質の現れ方が最も単純・典型的なので,金属学習の初めに扱うものとして適しているといえる。
(2)身近な物質を通して学ぶ
化学の時間に扱うものは,準備室の薬品棚に並んでいる試薬と生徒に思われていないだろうか。食塩やショ糖でさえ,試薬瓶に入っているものを使っていないだろうか。普段扱ったことのない薬品を使用し実験をすることも大切なことだとは思う。ときには,もっと身近なものを通して化学を学ぶことができれば,化学好きが増えるのではないだろうか。そして,身近な物質を通して学べば,身の回りのものを化学的視点から見ることができるようになり,確実に視野が広まると考える。
(3)高校教科書でのカルシウムの扱われ方
 啓林館「高等学校 化学I 改訂版」
啓林館「高等学校 化学I 改訂版」
「2族元素とその化学物」として約4ページ分の記述がある。化学反応式が8式に石灰水の白濁する様子の写真などが掲載され,丁寧に扱われている。具体例としては,鍾乳洞とセッコウ像さらにヒトの胃のレントゲン写真が載っている。
 アメリカの教科書
アメリカの教科書
「Addison-Wesley Chemistry」
The Alkaline Earth Metals として3ページ分の記述がある。反応式は3式。方解石・石灰岩・大理石・鍾乳石と並んでタージマハールの写真が載っている。さらに,炭酸カルシウムとして貝殻の写真も載っている。余談だが,マグネシウム関連として,アスベスト除去の写真も掲載されている。
3.教材開発
(1)身近なカルシウム化合物
道端に落ちている石の中には石灰石を含むものもある。チョークの主成分は,炭酸カルシウムや硫酸カルシウムなどである。貝殻や卵のからもカルシウム化合物である。グランドの白線には水酸化カルシウムや炭酸カルシウムなどが使われている。骨もカルシウムを含んでいる。このように,身近にカルシウム化合物は結構あるのだが,どれも白色系で見映えがしない。
また,石灰水に二酸化炭素を通すと白濁する実験に代表されるように,反応自体も地味であり,目玉となるような実験がない。
(2)反応物として乾燥剤を用いる
薬品棚にある試薬を用いてセッケンを作ったりナイロンを合成したりという,馴染みのない反応物から身近なものを合成する実験は多数おこなわれている。そこで,今回は逆に身近なカルシウム化合物を出発点(反応物)とした教材を開発した。
特に,興味・関心を高めるために,日常生活では禁止されているような実験を,最初に行い目玉とした。せんべいなどの袋の中に乾燥剤として使われている生石灰に水を加える実験である。禁水と書かれている乾燥剤の袋から中身を出し,水を加えるのである。禁止されていることができる,このワクワク感は,化学に興味を持たせるのにきわめて有効であると考えた。
4.授業実践
(1)乾燥剤(酸化カルシウム)
 乾燥剤
乾燥剤
 教室へお菓子を持って行き,黙って一口食べてから,
教室へお菓子を持って行き,黙って一口食べてから,
「この袋の中には,お菓子以外に,食べられないものが入っています。何か知っていますか?」
乾燥剤等の袋を取り出して,
「お菓子などの袋の中には,乾燥剤・脱酸素剤・かび防止剤などが入っています。その中で,一番多くの袋に入れられており,大きめなのが乾燥剤です。食べ物が湿気らないよう入れられているのです。乾燥剤として今一番使われているのは,石灰乾燥剤です。この袋にも石灰乾燥剤と書かれています。」
 生石灰
生石灰
 「この袋をはさみで切って中身を見てみましょう。どんなものが入っていると思いますか?」
「この袋をはさみで切って中身を見てみましょう。どんなものが入っていると思いますか?」
白い,硬い,かたまりが入っているのを観察。これが生石灰であることを説明。
 生石灰+水→消石灰
生石灰+水→消石灰
「袋には『禁水』と書かれています。水と反応させてはいけないということです。では,ビーカーにこの生石灰の粒を入れ,禁止されている水を少量加えたらどうなるでしょうか?」
生石灰に水を少量入れると,ゆっくりと反応が始まり,やがて大熱を出し水蒸気がもうもうと上がる様子を観察。
 消石灰+多量の水
消石灰+多量の水
「![]() のビーカーに水をたくさん入れ,よくかきまぜるたら,白色粉末はすべて溶けるでしょうか?」
のビーカーに水をたくさん入れ,よくかきまぜるたら,白色粉末はすべて溶けるでしょうか?」
多量の水を加えガラス棒でよくかき混ぜ牛乳のように白濁する様子,静置すると溶けきらない白色粉末が沈殿する様子を観察。


(2)消石灰(水酸化カルシウム)
 消石灰の自然乾燥
消石灰の自然乾燥
「(1)![]() のビーカーの底に沈殿した白色粉末は何でしょうか?取り出して自然乾燥させ,それに水を加えたら,(1)Bのときの様に発熱するでしょうか?」
のビーカーの底に沈殿した白色粉末は何でしょうか?取り出して自然乾燥させ,それに水を加えたら,(1)Bのときの様に発熱するでしょうか?」
 白色沈殿を取り出し,乾燥させ,その白色粉末に水を加えても反応(発熱)しないか実験。反応しないので,生石灰ではなくなったことを確認。生石灰に水を加えてできた白色粉末が「消石灰」であることを説明。
白色沈殿を取り出し,乾燥させ,その白色粉末に水を加えても反応(発熱)しないか実験。反応しないので,生石灰ではなくなったことを確認。生石灰に水を加えてできた白色粉末が「消石灰」であることを説明。
白色沈殿を塊にして,天日干しで自然乾燥させると,堅くなることも観察。
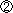 石灰の利用法
石灰の利用法
「これまで実験した生石灰に水を加えると発熱することなどを,実際の生活で利用している例を知っていますか?」 水との反応熱を利用して,ものを温める例。
「燗番娘」という,日本酒を反応熱で温めるもの紹介。生徒は弁当(駅弁)を温める例の方をよく知っていた。また,手品のネタとして使われている例も紹介。
 しっくいの例。
しっくいの例。
土蔵の漆喰壁や屋根瓦を接着などの例を紹介。消石灰が空気中の二酸化炭素と反応して石灰石に変化していることも説明。また,水中でしっくいは作業ができなかったため,1824年イギリスの煉瓦職人アスプディンが,雨が降っていてもかたまるようポルトランドセメント(ポルトランド島産の石灰石に色が似ていることから命名)を開発したことも紹介。
肥料の例。
作物を作り続けると酸性土壌になるこれを中和したり,カルシウム分を補給したりすることを説明。乾燥剤がだめになったら,畑にまくとよいことを紹介。
ここまでの反応を整理し,生石灰=酸化カルシウムCaO,消石灰=水酸化カルシウムCa(OH)2,石灰石=炭酸カルシウムCaCO3ということなどを説明。
(3)カルシウム(単体)
 Caの燃焼→生石灰
Caの燃焼→生石灰
カルシウムの単体を観察する。周期表上の知識でカルシウムは金属と知っていながらも,骨のイメージが強いため,金属光沢に生徒は驚いていた。
「このカルシウムを燃やすと,酸化カルシウム=生石灰になるでしょうか?」
Caを燃やし,できた白色物質に水を加える実験。激しく発熱し生石灰であることを確認。
(4)石灰石(炭酸カルシウム)
 石灰岩
石灰岩
石灰岩(石灰石)について説明。
 私たちの住んでいる富山県では県境付近に大量に産出する。生徒は,石灰岩搬出用の山から延びている長いベルトコンベーアを見たことがある。日本が自給できる数少ない鉱物である。大理石・貝殻・珊瑚・卵の殻・チョークなども炭酸カルシウムである。
私たちの住んでいる富山県では県境付近に大量に産出する。生徒は,石灰岩搬出用の山から延びている長いベルトコンベーアを見たことがある。日本が自給できる数少ない鉱物である。大理石・貝殻・珊瑚・卵の殻・チョークなども炭酸カルシウムである。
石灰石を強熱(900℃以上)すると,生石灰ができる。県境にあるセメント工場にある巨大な円筒形をしたものはキルンと呼ばれ,この反応をおこすための装置であることなどを説明。
 石灰石+塩酸
石灰石+塩酸
チョークや貝殻に,塩酸を加えて気体が発生する様子を観察。
「この気体の正体は何でしょうか?また,それを調べるには何を使うとよいだろうか?」
二酸化炭素と予想。したがって調べるには石灰水が必要。ここで,(1)![]() の消石灰溶液の上澄みを使って実験するよう指示。上澄みの透明部分に消石灰が溶けており,石灰水であることを理解。
の消石灰溶液の上澄みを使って実験するよう指示。上澄みの透明部分に消石灰が溶けており,石灰水であることを理解。
石灰石(炭酸カルシウム)を強熱すると生石灰(酸化カルシウム)になる,生石灰(酸化カルシウム)に水を加えると消石灰(水酸化カルシウム)になる,消石灰(水酸化カルシウム)に二酸化炭素を加えると石灰石(炭酸カルシウム)になる,という循環を確認。
 石灰水+過剰の二酸化炭素
石灰水+過剰の二酸化炭素
石灰水に二酸化炭素を通すと,炭酸カルシウムの白色沈殿ができる実験は,中学までに何度も経験している。そこで,さらに過剰に二酸化炭素を加え,無色透明な溶液(炭酸水素カルシウム)になる実験。そして教科書の鍾乳洞の写真等を参考に,この反応により石筍が形成されたりすることを考察。
5.授業分析
(1)生徒による授業評価
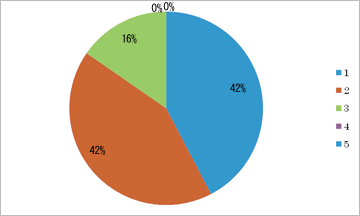
この授業は楽しかったですか?
- たいへん楽しかった 33名
- 楽しかった 33名
- どちらともいえない 12名
- あまり楽しくなかった 0名
- 全然楽しくなかった
8割以上の生徒が,この授業はたいへん楽しかった・楽しかったと評価している。
(2)感想
- Y.R.(女)
- 身近なことがけっこうでてきたので,日頃自分で何気なく見ているものが,こういう裏付けがあるのだなあーって思った。また,この前テレビで消石灰と生石灰について出ていて,自分は知っているみたいな感じでうれしかった。
- Y.H.(男)
- これまであまり意識してこなかったけれど,石灰石は意外と身近で,様々に使用されているということがわかった。コンクリートの色や性質などについての不思議を自分なりに解決することができた。
- I.K.(男)
- 石灰は身近にあるものと思っていたが,想像以上に知らないことが多く,初めて知ることもたくさんあった。生石灰と消石灰の違いなど,わかりそうでわからなかったことを学べてよかった。
- T.K.(男)
- 今回一番おもしろいと感じたのは生石灰から消石灰になるとき,ものすごい熱が出るということです。身近なところに,そのような危険なものがあるとは思っていませんでした。危険だけどかなりおもしろそうなので,自分でもやってもたいと思いました。
- S.A.(女)
- まず一番驚いたことというか,意外だったことは,石灰水に二酸化炭素を吹き込んで 透明→白→薄くなる という変化をすることでした。ずっと白いままではないのですね!!また,大理石と石灰が関係あるものだとは思っていなかったので,つながりを感じて楽しかったです。
- N.K.(女)
- 石灰岩が様々反応を起こして,最終的には石灰岩にもどるというのが,すごくおもしろかったです。石灰と言ったら,グラウンドにラインを引くときのものしか知らなかったけれど,石灰の性質を利用して,肥料やお弁当を温めたりすることに使われるなど,身近なところにもたくあるのだなと思いました。このように,身近なことで化学の勉強をすると,とても楽しかったです。
- T.M.(女)
- 畑の肥料である白い粉と大理石の原料が同じものだと知って,びっくりした。
「石灰水に二酸化炭素を通すと白濁する」と教えられてきたけど,その理由がわかってよかった。 - U.K.(女)
- 生石灰の話からどんどん広がっていって,でも,化学反応式を見ると繰り返しという感じがして,不思議でした。お弁当やお酒,大理石など身近なものにも関係しているのだなと思いました。扱いに注意しなくてはならないものもわかったので気をつけたいです。
- N.K.(女)
- まず,石灰に種類があることを初めて知った。なかでも,大理石でできた建物が火事になり生石灰ができ,雨が降ると消石灰になるというのは,すごい性質だと思った。身の回りにある石灰でできたものを改めて見てみたい。
- T.K.(女)
- 鍾乳洞は本物を見たときも解説されたが,1年でほんの少ししかできないものが,あそこまで大きくなるなんてすごいなあと思ったものだった。今,石灰の話を聞いて,よけいに石灰の不思議が少しわかった気がした。
- I.J.(男)
- 自分の知っていることから知らないところに踏み込んでいくのはおもしろかった。石灰水に過剰に二酸化炭素を入れると透明にもどるというのには驚いた。
(下線は,授業者がつけたものである。)
6.授業を受けた生徒による課題研究
(1)テーマの決定
4の授業を受けカルシウム化合物に強い興味・関心を持った生徒達が,「ごみを生かす」という読売新聞の特集記事を読み,国内で年間21万トンにもなるホタテの廃棄貝殻を焼いて酸化カルシウムなどとして再利用されていることを知り,「炭酸カルシウムの熱分解」というテーマで課題研究に取り組んだ。
 (2)研究の概略
(2)研究の概略
高性能卓上マッフル炉を使用し,加熱時間と熱分解の関係,加熱温度と熱分解の関係を調べた。
貝殻や鶏卵殻などを加熱し,酸化カルシウム等に変化するか調べた。
(3)実験方法
 炭酸カルシウムの加熱
炭酸カルシウムの加熱
- 電子天秤で炭酸カルシウムの質量を測定する。 ag
- マッフル炉に加熱温度・時間等のプログラムを入力し,炭酸カルシウムを加熱する。
- 自然冷却し,質量を測定する。 bg

 生成物の確認
生成物の確認
- 水を加え,熱の発生を確かめる。
- 水溶液の液性を確かめる。
- 塩酸を加え,二酸化炭素の発生を確認する。
- 加熱前の炭酸カルシウムの質量agより,完全に熱分解されたとき生成される酸化カルシウムの質量 Wgを求め,実際生成した質量 bgの割合(百分率)を求める。
(4)結果
生徒のデータを表1・2に示す。
表1 温度による反応の違い
| 時間(h) | 温度(℃) | a(g) | b(g) | c(g) | b/W(%) | 水との反応 | 塩酸との反応 | pH |
|---|---|---|---|---|---|---|---|---|
| 8 | 900 | 18 | 10.8 | 10.08 | 107.1429 | 熱発生 | CO2発生せず | ― |
| 8 | 900 | 10.37 | 6.1 | 5.8072 | 105.042 | 熱発生 | CO2発生せず | ― |
| 4 | 900 | 9.6 | 5.45 | 5.376 | 101.3765 | 熱発生 | CO2発生せず | ― |
| 4 | 800 | 15.2 | 9.91 | 8.512 | 116.4239 | 熱発生 | CO2発生せず | 13 |
| 4 | 700 | 10.61 | 9.69 | 5.9416 | 163.0874 | 熱発生せず | CO2発生 | 13 |
| 4 | 600 | 14.24 | 14.14 | 7.9744 | 177.3714 | 熱発生せず | CO2発生 | 11 |
| 4 | 500 | 11.66 | 11.63 | 6.5296 | 178.112 | 熱発生せず | CO2発生 | 7 |
| 4 | 300 | 9.78 | 9.77 | 5.4768 | 178.3888 | 熱発生せず | CO2発生 | 11 |
表2 時間による反応の違い
| 時間(h) | 温度(℃) | a(g) | b(g) | c(g) | b/W(%) | 水との反応 | 塩酸との反応 | pH |
|---|---|---|---|---|---|---|---|---|
| 8 | 900 | 18 | 10.8 | 10.08 | 107.1429 | 熱発生 | CO2発生せず | ― |
| 8 | 900 | 10.37 | 6.1 | 5.8072 | 105.042 | 熱発生 | CO2発生せず | ― |
| 4 | 900 | 9.6 | 5.45 | 5.376 | 101.3765 | 熱発生 | CO2発生せず | ― |
| 4 | 800 | 15.2 | 9.91 | 8.512 | 116.4239 | 熱発生 | CO2発生せず | 13 |
| 4 | 700 | 10.61 | 9.69 | 5.9416 | 163.0874 | 熱発生せず | CO2発生 | 13 |
| 4 | 600 | 14.24 | 14.14 | 7.9744 | 177.3714 | 熱発生せず | CO2発生 | 11 |
| 4 | 500 | 11.66 | 11.63 | 6.5296 | 178.112 | 熱発生せず | CO2発生 | 7 |
| 4 | 300 | 9.78 | 9.77 | 5.4768 | 178.3888 | 熱発生せず | CO2発生 | 11 |
7.まとめ
音や光を伴うような印象的な実験があるわけでもなく,化学の教師にとっては一つ一つの実験は既知のものかもしれない。だがしかし,身近な物質を出発点とし,実生活と結びつくよう展開を工夫しただけで,生徒の評価に現れているように楽しく意欲的に学ぶことができる授業とすることができた。
また,生徒の感想から読み取れるように,「理科を学ぶことの意義や有用性を実感する機会をもたせ,科学への関心を高める観点から,実社会・実生活との関連を重視する内容を充実させる方向で改善を図る。」(中央教育審議会答申「学習指導要領等の改善について」平成20年1月17日)というねらいを具現化した授業となった。
8.参考文献
- 中央教育審議会 初等中等教育分科会 教育課程部会「教育課程部会におけるこれまでの審議のまとめ」(平成19年11月7日)
- 中央教育審議会「学習指導要領等の改善について」答申(平成20年1月17日)
- 齋藤烈ほか『高等学校化学T改訂版』啓林館(2008)
- Antony C. Wilbraham『Chemistry』Addison-Wesley (2002)
- 重松栄一『化学』民衆社(1996)
- 富山高校化学班「炭酸カルシウムの熱分解」富山県理数科課題研究集録(2007)
- きた産業ホームページ
- 明星セメントホームページ
|
|||